本レポートに掲載した銘柄
ヘリオス(4593)/大日本住友製薬(4506)/サンバイオ(4592)/武田薬品工業(4502)/タカラバイオ(4974)
薬品・バイオ株コメント:再生医療関連
1.iPS細胞の臨床研究再開へ
iPS細胞は、人間の様々な細胞(皮膚、内臓などに専門化した細胞)を一旦「初期化」することによって、再び様々な細胞になることが出来る「万能細胞」です。ほぼ無限に増殖できるという特徴もあります。
2006年に京都大学の山中教授(2012年ノーベル賞受賞)がマウスからのiPS細胞作成に成功し、2007年にはヒトiPS細胞の作成に成功しました。更に、2014年9月には理化学研究所(理研)の高橋博士が加齢黄斑変性(滲出(ウェット)型)の治療のために、患者のiPS細胞から「網膜色素上皮細胞」を作成し、患者に移植しました。その後の経過は良好で、患者の視力低下は止まり、合併症、拒絶反応がなく、腫瘍にもなっていません。
ただし、15年に予定していた2例目は、作成したiPS細胞にがん関連遺伝子の変異が見つかったため、中止となりました。iPS細胞の問題はこの「癌化」リスクであり、このことは株式市場にも影響しました。
このiPS細胞を巡る取り組みが再び前進しようとしています。6月6日、理研などのグループ(理研、神戸市立医療センター中央市民病院、大阪大学、京都大学iPS細胞研究所)は、加齢黄斑変性(ウェット型)に対してiPS細胞から育てた細胞を移植する臨床研究を再開すると発表しました。前回のような患者から作成したiPS細胞(自家細胞)だけでなく、他人から作ったiPS細胞(他家細胞)からも網膜色素上皮細胞を作成し患者に移植します。来年前半の移植実施を目指します。報道によれば約20名の患者に投与する見通しで、費用は大幅に低下する見込みです。
癌化リスクについては、iPS細胞の製作法の技術進歩によってほぼなくなっている模様です。また、眼はもともとがんになりにくい部位です。
2.iPS関連、再生医療関連企業への影響
ヘリオス
理研などのグループの加齢黄斑変性に関する臨床研究再開は、薬品・バイオ株に大きな意味を持ちます。ヘリオスは2013年2月に京大のiPSアカデミアジャパンから網膜色素上皮細胞にかかるiPS細胞に関する特許実施許諾権を受けています(全世界、非独占的ライセンス)。また同年3月、理研との間でiPS細胞を含む多能性幹細胞由来の網膜色素上皮細胞に関する特許実施許諾権を受けています(全世界、独占的ライセンス)。ヘリオスも2017年以降に、日本でiPS細胞から作った網膜色素上皮細胞を加齢黄斑変性の患者に移植(注射)する臨床試験(大日本住友製薬と共同開発)を開始すると思われます。その後はアメリカと欧州でも始めると思われます(単独開発か共同開発か未定)。
先週の本稿ではヘリオスについて、加齢黄斑変性治療薬(表1のHLCR011、HLCR012)の臨床試験開始に時間がかかりそうだとコメントしました。会社側は現時点で日本でのフェーズⅡ入りを2017年以降としていますが、理研グループが臨床研究を再開するのであれば、早ければ2017年中にも臨床試験入りする可能性があると思われます。
また、欧米での臨床試験(国際共同治験になる可能性があります)は、日本で開始した後、早期に開始される可能性があります。
先週も書きましたが、重症患者の数と予想される薬価(今の治療費は1年間約100万円なので、それ以上?)を考えると、ヘリオスの加齢黄斑変性治療薬は上市後数年で日米欧で各々1,000億円以上の市場に成長する可能性があります。これまで研究段階だったiPSが、今回の臨床研究再開をきっかけとして、現実の市場になるのも近いのではないかと思われます。
表1 ヘリオスの開発パイプライン
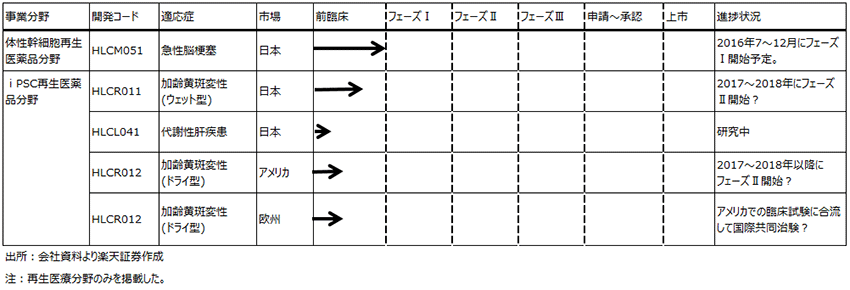
表2 加齢黄斑変性の罹患者数
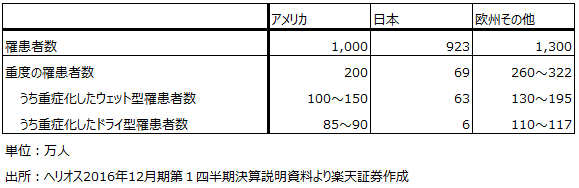
大日本住友製薬
大日本住友製薬はiPSなどの再生医療に関して、大学、研究機関では理研、京大、慶応大、企業(バイオベンチャー)ではへリオス、サンバイオと提携しています。iPS関連のみならず再生医療全体で広範囲に提携関係を結んでいる会社です。
大日本住友製薬は日本の他の大手、準大手製薬会社よりも、iPSを中心とする再生医療への取り組みが早かった会社です。これには理由があり、当社の主力薬である抗精神病薬「ラツーダ」が主要市場であるアメリカで2019年1月に特許切れとなるためです。ラツーダは2018年3月期~2019年3月期のピーク年商が1,500億円程度と予想される大型品ですが、そのため、これの特許切れは業績への影響が大きいのです。
逆に、業績への危機感から再生医療分野での各種提携を進めてきた結果、ヘリオスとの日本における加齢黄斑変性治療薬の共同開発と共同製造・販促会社の設立、サンバイオの再生細胞薬「SB623」のアメリカにおける共同開発と販売権獲得といった、2020年3月期以降の業績にとって重要なパートナーシップを獲得することができています。今後の展開に注目したいと思います。
表3 大日本住友製薬の再生・細胞医薬分野 事業化計画(2016年5月更新)
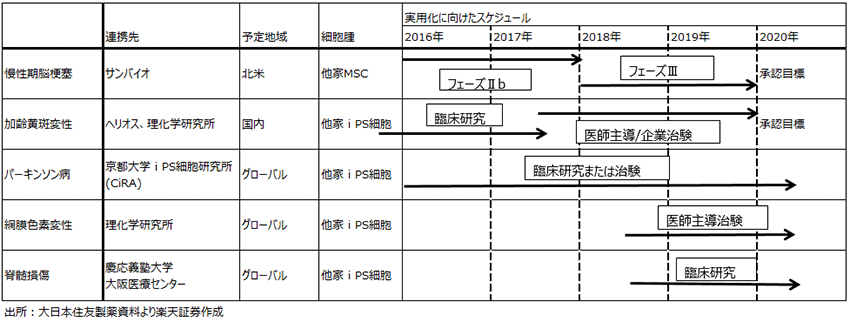
サンバイオ
今回の加齢黄斑変性の臨床研究再開は、株式市場では単にiPS関連企業だけでなく、再生医療関連企業全体の評価を上げるものです。
サンバイオの再生細胞薬「SB623」は、慢性期脳梗塞の臨床試験がアメリカでフェーズⅡbに入りました(大日本住友製薬との共同開発)。外傷性脳損傷の臨床試験(サンバイオ単独)はアメリカでフェーズⅡが始まり、日本も治験者を集めているところです。日本ではフェーズⅡの結果が良ければそのまま申請、承認、上市へ進めるため、2020年頃には日本で上市される可能性があります。
慢性期脳梗塞、外傷性脳損傷ともに患者数が多いため(脳卒中の患者数はアメリカ680万人、日本123万人、外傷性脳損傷は推定でアメリカ約250万人、日本40~50万人)、治療薬の市場規模は早期に日米各々1,000億円を超える可能性があります。ヘリオスの加齢黄斑変性治療薬もそうなると思われますが、再生医療の分野に限らず、これまで根治治療薬がなかったところに治療薬が出来ると、比較的高い薬価が認められる、あるいは値付けできる傾向にあるため、予想される市場規模が膨らむ傾向があります。
加齢黄斑変性、脳梗塞のほか、将来予想されるパーキンソン病などの分野まで含めて考えると、サンバイオ、ヘリオスのような再生医療関連企業の将来の企業価値は今よりも更に大きくなることが予想されます。
表4 サンバイオの開発パイプライン
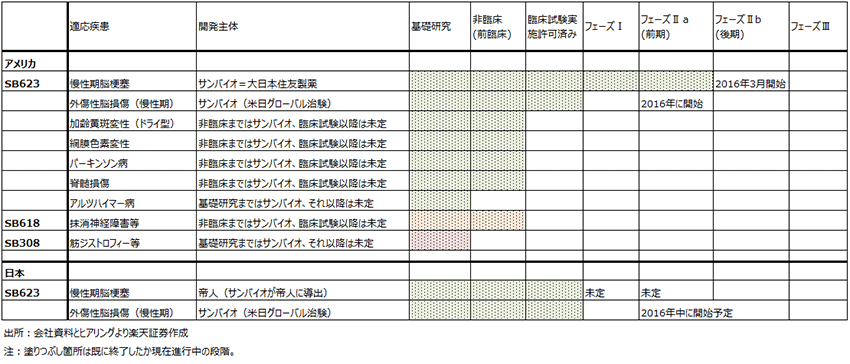
この他、次のような企業群が重要な動きをしています。
武田薬品工業
2015年4月に京都大学iPS細胞研究所(CiRA、サイラ)と10年間の共同研究契約を締結しました。武田薬品工業が10年間で200億円の資金提供をCiRAに対して行い、同社湘南研究所の中に拠点を提供します。プロジェクトは京大山中教授が直接主導し、生み出された知財は両者で共有します。武田薬品工業にとってはiPS関連で大手になるチャンスです。
富士フイルムホールディングス
2014年12月にジャパン・ティッシュ・エンジニアリングを連結子会社化しました。同社は、日本の再生医療等製品として1、2番目に承認された「自家培養表皮ジェイス」(重症熱傷を治療するための自家再生表皮)、「自家培養軟骨ジャック」(膝関節における外傷性軟骨欠損症又は離断性骨軟骨炎(変形性膝関節症を除く)の臨床症状の緩和を目的とする)を開発した企業です。
また、2015年5月に米セルラー・インデックス・インターナショナル(CDI)を約3億ドルで買収しました。CDIはiPS細胞を大量かつ安定生産する技術を持つ会社です。
富士フイルムホールディングスにとって医薬品分野は重要分野ですが、再生医療でも重要な動きをしています。
タカラバイオ
2014年8月に、iPS細胞などの幹細胞を肝細胞や膵臓細胞などに分化させる分化誘導技術や、ES細胞、iPS細胞、分化細胞など幹細胞に関連する製品を持つスウェーデンのセレクティス AB社(現タカラバイオ・ヨーロッパAB)を買収しました。この分野では大手で知名度があるため、タカラバイオのバイオ産業支援事業の拡大に寄与しています。
テルモ、JCRファーマ
この両社とも再生医療製品を上市しています。テルモは、2016年5月に「ハートシート」を発売しました。ハートシートは、患者の大腿部から採取した筋肉組織に含まれる骨格筋芽細胞を培養して、シート状に調製し心臓表面に移植する製品で、虚血性心疾患による重症心不全の治療に使います。
また、JCRファーマは2016年2月に、間葉系幹細胞を用いた移植片対宿主病治療製品「テムセルHS注」を発売しました。この2つの製品は、2015年9月に承認された再生医療等製品です。
リプロセル
現在の主力事業はiPS関連の研究試薬の製造販売と創薬支援ですが、将来は再生医療に展開する計画です。
このようにiPS関連、再生医療関連には幅広い分野の企業がかかわっています。
3.日本政府も積極支援
再生医療分野へは政府も積極的に支援しています。2014年11月に施工された改正薬事法では、再生医療等製品の早期承認制度が設けられました。短期間で当該製品の有効性が推定されれば、条件付、期限付きで承認されることになりました。これによって、従来はフェーズⅢまで必要だった臨床試験がフェーズⅡ終了で申請できることになりました。フェーズⅠ、Ⅱと3~4年で申請できることになり、諸外国の中でも日本はバイオベンチャー(特に再生医療関連のバイオベンチャー)にとって優しい国となったのです。また支援のための予算もできました。
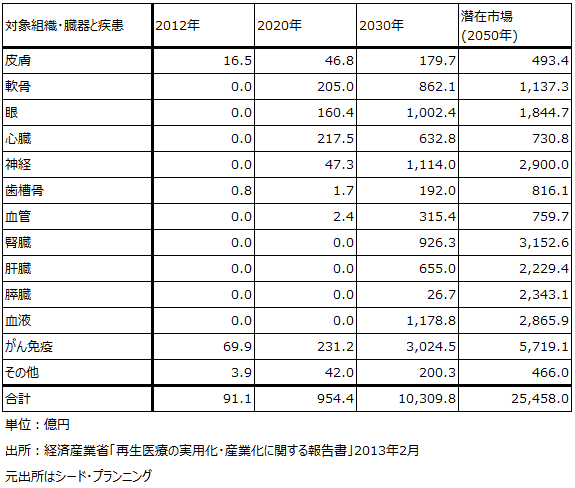
なお、経済産業省の「再生医療の実用化・産業化に関する報告書」(2013年2月)によれば、国内の再生医療の市場規模は、2012年91億円から2020年954億円、2030年1兆310億円に拡大すると予想されます。これは少し古い数字ですが、上述のような各主要企業の開発動向と患者数から見ると、例えば、加齢黄斑変性と慢性期脳梗塞あるいは外傷性脳損傷で、2030年までに各々1,000億円以上の市場になってもおかしくないと思われます(上記の報告書では、2030年の市場規模が加齢黄斑変性滲出型(ウェット型)、萎縮型(ドライ型)合わせて732億円、脳梗塞が509億円)。がん免疫療法に対する再生医療の応用のように、まだ不透明な分野もありますが(同3,025億円)、多くの分野で予想以上の速さで再生医療が実用化される可能性があります。また、この報告書では、再生医療の世界市場は2030年に12兆円に拡大すると予想されています。
投資について考えると、再生医療関連の中で、患者数の多さ、上市後予想される売上高の大きさを考えて、ヘリオス、サンバイオに中長期で注目したいと思います。同様にこの2社と提携関係にある大日本住友製薬にも注目したいと思います。
また、タカラバイオは上述の様なiPS関連産業向け事業だけでなく、広い意味での再生医療と言える遺伝子治療で日本有数の会社です。抗ガン剤中心に創薬へも注力しており、投資妙味を感じます。
薬品・バイオ株には好材料が継続して出ています。引き続き注目したいと思います。
表5 再生医療の市場規模(国内)
グラフ1 再生医療の将来市場規模予測(世界)
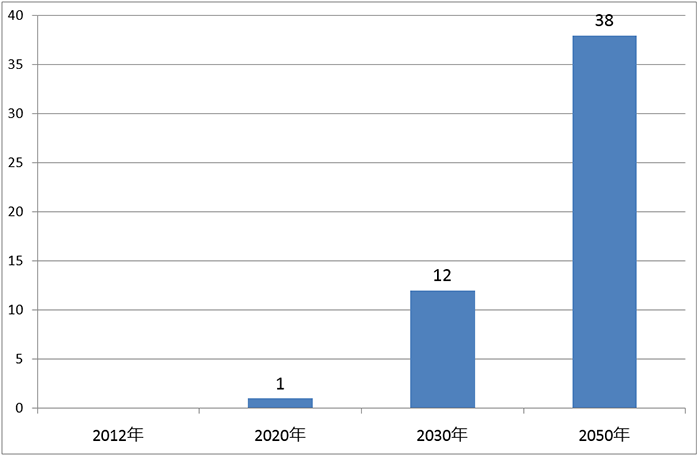
(単位:兆円、出所:経済産業省)
本レポートに掲載した銘柄
ヘリオス(4593)/大日本住友製薬(4506)/サンバイオ(4592)/武田薬品工業(4502)/タカラバイオ(4974)













![[動画で解説]成長株、割安株、高配当利回り株…どの株を選べばいい?](https://m-rakuten.ismcdn.jp/mwimgs/8/4/498m/img_84b60a4da51373f73b5c52275b097f2837381.jpg)













![[動画で解説]桐谷さんの優待生活に突撃!#1~桐谷さん、おきに優待ベスト3見せてください!~](https://m-rakuten.ismcdn.jp/mwimgs/9/5/498m/img_9528c8c2f23001a3deb43de0c6f7845872398.jpg)




















![[今週の日経平均]最高値更新も「天井サイン」出現!今週の日本株どうなる?!](https://m-rakuten.ismcdn.jp/mwimgs/2/b/160m/img_2b5a074cc6a3e935645125fb974dffcf59165.jpg)


![[動画で解説]みずほ証券コラボ┃7月16日【米株は小型選別 日本株はドル建てに注目~今週は米共和党大会と米決算発表~】みずほウィークリーVIEW 中島三養子](https://m-rakuten.ismcdn.jp/mwimgs/2/a/498m/img_2a5df0131378bd46a83ce1f01fbb418d92438.jpg)
![[動画で解説]【テクニカル分析】今週の日本株 最高値を更新後日本株はどうなる?~出現した「天井サイン」をどう読むか~<チャートで振り返る先週の株式市場と今週の見通し>](https://m-rakuten.ismcdn.jp/mwimgs/6/0/498m/img_60df7a3c9e52ac000de20f75f870968d71371.jpg)
![[動画で解説]円高ショックで日経平均急落、夏枯れ相場始まり?](https://m-rakuten.ismcdn.jp/mwimgs/3/c/498m/img_3c55226b36153bdd05e3d3a674f68f9245072.jpg)
![[動画で解説]新NISAを使った個別株投資について](https://m-rakuten.ismcdn.jp/mwimgs/0/c/498m/img_0c14e3a2b5e84beb52872a9b879aa3e795587.jpg)




















![[今週の日経平均]最高値更新も「天井サイン」出現!今週の日本株どうなる?!](https://m-rakuten.ismcdn.jp/mwimgs/6/c/356m/img_6c199645af38ea98963a94af8b6f3b6934054.jpg)
























![[動画で解説]日銀が7月利上げに踏み切るべきでないこれだけの理由](https://m-rakuten.ismcdn.jp/mwimgs/a/8/160m/img_a8715b638366eed8a8f8d75613b8e92163161.jpg)




