本レポートに掲載した銘柄
小野薬品工業(4528)
小野薬品工業
1.特例によるオプジーボ薬価引き下げの動き
今回は、小野薬品工業の最近の動きをまとめ、当面の株価動向を考えます。
まず、高額医薬品の薬価を巡る動きからです。今年の春から、オプジーボの高額薬価に関する議論が活発になっており、中央社会保険医療協議会総会と同薬価専門部会において、7月から本格的な議論が行われています。今の流れでは、10月中に方向性を決めるということです。スケジュールを考えると、年内にもオプジーボについて特例的な薬価引き下げがあるか、遅くとも2017年4月までに引下げとなる可能性が高いと思われます。
今後の問題はオプジーボの薬価引下げ率です。適用する制度が「特例市場拡大再算定」か、「用法用量変化再算定」かで引下げ率が異なります。特例市場拡大再算定であれば、会社予想の今期売上高が1,260億円で、薬価改定の際に厚生労働省が推計するオプジーボの年間市場規模も大きな違いはないと思われることから、最大25%引下げとなる可能性があります(表1)。
一方で、用法用量変化再算定を採用するならば、55.6%というかなり大きな引下げ率となる可能性があります(表2)。
10月中に議論の中身が明らかになると思われますが、どちらになるかは、正式な決定を待つしかありません。薬価引き下げの時期も同様ですが、ここでは業績予想の便宜上もあって、2017年4月の引き下げと予想しています。
私の意見ですが、オプジーボの薬価が国際比較しても高いことを考えると、今後2年間で半値程度への引下げは避けられないのではないかと思われます。オプジーボの価格は、1瓶当たりではアメリカの約3倍、1人当たりの月間使用金額は同じく約2倍です(日本は標準体重60kg、アメリカ人は80kgで換算する)。もともとは、アメリカに比べて患者数が大幅に少ないメラノーマ向けに設定された薬価なので、想定年間投与者数が15,000人の非小細胞肺がん向けに長続きする薬価ではないと思われます。ただし、いきなり50%以上の価格引下げは小野薬品の事業意欲、ひいては日本の製薬メーカーの新薬開発意欲を打ち砕くことになりかねないため、25%程度の値下げが適当かと思われます。
また、後述の業績試算のように、2018年4月の定例の薬価改定時にも引下げが予想されます。2017年4月に25%引下げなら、2018年3月期は腎細胞がん、頭頸部がんへの適用拡大による投与人数増加と継続投与患者の増加によって、オプジーボの売上高が1,500億円以上になることが予想されるためです。一方で、引き下げ率が55.6%の場合、来期のオプジーボ売上高は1,000億円を下回る可能性があるため、2018年4月の引下げはないか、より軽いものになると思われます。
この問題は複雑で、日本医師会のように、オプジーボの薬価引下げ分を診療報酬点数の引き上げ原資として使うように求める団体もあります。診療報酬点数の改定は薬価改定と同時期なので、この意見がある程度反映される場合は、2017年4月よりも2018年4月に重点をおいた引下げになる可能性もあります。
いずれにせよ、2017年4月までの薬価引下げは不可避と思われます。
表1 特例市場拡大再算定

表2 用法用量変化再算定

2.非小細胞肺がんファーストラインへの道筋
8月にブリストル・マイヤーズ スクイブ(BMS)と小野薬品工業は両社の国際共同治験である、「CheckMate-026」試験が失敗した旨のリリースを出しました。CheckMate-026は非小細胞肺がんのファーストライン(ステージⅣの患者に対する最初の薬)のための臨床試験(フェーズⅢ)です。これまでオプジーボに関する臨床試験は全て成功してきましたが、初めての失敗です。薬価引下げの議論が盛んになった中での026試験の失敗により、株価は大きく下落しました(8月12日付け楽天証券投資WEEKLYを参照)。
がん治療薬が最初の臨床試験を終えて承認、上市となった時は、セカンドライン(通常の抗がん剤などの他の薬による治療を行った後の治療)以降の投与となります。がん治療薬は劇薬なので、最初からファーストラインではなく、その後の臨床試験を経てからファーストラインとして申請することになります。026試験の結果は、既存薬に対して無増悪生存期間(Progression-Free Survival、PFS、治療後がんが進行せず安定した状態である期間のこと。進行がんの患者に対する治療効果を見るときによく使われる)で統計上優位な差が見られなかったということでした。つまり失敗です。他の評価項目である全生存率(OS)、奏効率(ORR)については、年内にも開示されると思われます。
ただし、オプジーボの「効果」がなかったわけではありません。効果はありましたが、既存の化学療法剤や分子標的薬と比べて、際立った効果はなかったということです。非小細胞肺がんは治療が難しいがんですが、患者数が多く市場が大きいため、優秀ながん治療薬が既に上市されているという事情があると思われます。026試験でオプジーボの比較対象となったのは、ゲムシタビン、シスプラチン、カルボプラチン、パクリタキセル、ペメトレキサド(いずれも一般名)の5種類です。
非小細胞肺がんファーストラインについては、026試験以外にCheckMate-227試験が進行中で、2018年1月に終了する予定です。これも026試験同様、BMSとの国際共同治験です。これが成功すれば、この結果をもってファーストラインを申請する予定です。ただし、これにも失敗するようであれば、小野薬品としては、BMSとの国際共同治験をあきらめ、日韓台を対象とした単独の臨床試験を行う方針の模様です。
競合するメルクの「キイトルーダ」(一般名ペムブロリズマブ)も、まだ日米欧で非小細胞肺がんのファーストラインは承認されていません。ただし、臨床試験では良好な結果が得られており、アメリカのFDA(アメリカ食品医薬品局)からブレイクスルーセラピーの指定を受け、優先審査の対象となっています。審査期日は2016年12月24日です。キイトルーダは、アメリカではメラノーマのファーストラインと非小細胞肺がんのセカンドライン以降で上市されており、日本では9月28日付けでメラノーマ向けが承認されました。申請中の非小細胞肺がんセカンドラインも年内には承認されると思われます。
キイトルーダとオプジーボの競合関係がどうなるかについては、株式市場では意見が分かれていると思われます。私の意見ですが、キイトルーダの非小細胞肺がん向けはPD-L1発現率50%以上の制約があるため、この制約がないオプジーボに比べて対象患者数は少なくなります(推定でオプジーボの4分の1程度か)。また、医師は使いなれた薬品を選ぶ傾向があるため、セカンドラインの場合はキイトルーダ上市の影響は考えにくいと思われます。キイトルーダのファーストラインが日米欧で承認されても、PD-L1発現率50%以上の制約は残るため、影響は少ないと思われます。
一方で、患者数の多い非小細胞肺がん向けのファーストラインでキイトルーダに先を越されると、オプジーボにはネガティブな影響があるという意見もあります。これは、実際にキイトルーダのファーストラインが承認された後でなければわかりません。
今後のオプジーボの投与者数を予想すると、非小細胞肺がんファーストラインが当面なくなったのは残念ですが、2018年3月期から非詳細肺がんセカンドライン向けの本格展開が始まり(今期は慎重に投与する医師、病院が多く、小野薬品も慎重投与を呼び掛けているため、会社予想の非小細胞肺がん新規投与者数15,000人を下回ると思われる)、腎細胞がん、頭頸部がんが加わり、2019年3月期から胃がん、肝細胞がんなどが加わると思われます(ただし、227試験以外の現在進行中の臨床試験が全て成功するという前提です)。非小細胞肺がんファーストラインが実現すれば、年間の新規投与者数が1万人程度増えると思われますが、これがなくとも当面の投与人数は増え続けると思われます。
表3 オプジーボの臨床試験スケジュール(主なもの)

3.併用剤、併用療法の開発動向
現在のところ、小野薬品の併用剤の開発は、BMSのヤーボイ(イピリムマブ)との併用を優先しています。ヤーボイは4回の投与で治療が終了するため、オプジーボのように継続投与に伴う費用の高額化はある程度避けることは出来ますが、ヤーボイの投与に4回で728万円かかるため(メラノーマの場合)、オプジーボと合わせるとやはり高額になります。
併用剤、併用療法の開発で注目したいのは、次の臨床試験または他社の開発パイプラインです。
- CheckMate227試験(非小細胞肺がんファーストライン、フェーズⅢ)でのオプジーボ単剤とオプジーボ+ヤーボイの併用、オプジーボとゲムシタビン、シスプラチン、カルボプラチン、ペメトレキサドとの併用の比較試験。2018年1月終了予定。
- 膠芽腫に対する放射線療法とオプジーボの併用療法(フェーズⅢ)。BMSとの国際共同治験で2019年3月終了予定。がん放射線療法では、放射線を照射したがんだけでなく、 照射部位から離れたところに転移したがんが縮小するケースが見られており、放射線による免疫活性化の可能性が指摘されている。そこで放射線療法とオプジーボと併用することで、更に免疫を活性化して、がんの治療効果を上げようと言うもの。
- タカラバイオが開発中の腫瘍溶解性ウイルス「HF-10」のメラノーマ向けフェーズⅡ(今期中に開始予定)で、免疫チェックポイント阻害剤との併用が検討されている。
- グリーンペプタイドが開発中のがんペプチドワクチン「GRN-1201」(メラノーマ向け)でも免疫チェックポイント阻害剤との併用が検討されている。
これ以外で重要なのは、オプジーボが効く患者を見つけるためのバイオマーカーの開発です。9月16日付けで小野薬品が公表した国立がん研究センターとの包括的研究提携契約の骨子は、新たな抗がん剤の創出とがん免疫療法におけるバイオマーカーの探索です。「新たな抗がん剤の創出」とは、オプジーボ後の新薬開発とオプジーボの併用剤開発の両方が含まれると思われます。バイオマーカーの探索については、オプジーボの作用機序には未解明の部分が多くあり、PD-L1発現率の高い患者にターゲットを絞るだけでは、奏効率を上げるには不十分だからです。
今の臨床試験のスケジュールでは、CheckMate227試験が2018年1月終了、膠芽腫と放射線療法の併用療法の臨床試験が2019年3月終了予定です。これらの臨床試験が成功すれば、2020年3月期以降併用剤、併用療法が本格化し、オプジーボの需要が増える要因が出来ると思われます。
4.メルクとの訴訟について
キイトルーダを開発、販売しているメルク(Merck)とは、「抗ヒトPD-1抗体によるがん治療を目的とした用途特許」(特許権者はオプジーボの研究者である本庶佑(ほんじょ・たすく)氏と小野薬品工業)について欧米各国で係争中です。欧州では、メルクが小野薬品、BMS、本庶氏を特許無効で訴えて、小野薬品とBMSがメルクに対して特許侵害訴訟を起こしています。第一審判決は、欧州特許庁(2014年6月)、イギリス(2015年10月)、オランダ(2016年6月)ともに特許有効判決が出ており、メルク側は各々控訴しています。
アメリカでは、小野薬品、BMS、本庶氏が、メルクに対して、2014年9月に特許権侵害訴訟を起こしています。2016年5月にマークマン ヒアリング(Markman Hearing、特許請求項の解釈を行うためのもの。両当事者が様々な書類を提出する)が行われており、2017年4月にTrial(トライアル、証拠開示で入手した情報に基づき、訴訟の争点に関係する具体的な事実が明らかになる。日本の「公判」に相当)が予定されています。
日本では、キイトルーダが上市されていないため、訴訟は起きていません。しかし、既に承認されたため、上市され次第、小野薬品などが何らかの法的措置を講ずると思われます。
5.2017年3月期~2019年3月期の業績試算
今後実施されるであろうオプジーボへの特例的薬価引下げと、非小細胞肺がんファーストラインが当面なくなったことを織り込んで、今後の業績を試算しました。表5の前提1は薬価の前提で、2017年4月にオプジーボの薬価が25%引下げになって、その後も定例の薬価改定時に引下げがあると想定しました。同じく前提2は、2017年4月に55.5%の値下げがあるとしました。
2018年4月以降の定例の薬価改定時のオプジーボの薬価引下げ率は、その前年度の売上高に左右されます。ここでは、特例拡大再算定の基準に従って値下げ率が決まるとしました。ただし、年間売上高1,500億円以上の場合でも、50%引下げはないとしました。これは、それほど大きな値下げを行った場合、企業側が事業の継続する意思を失う恐れがあるためです。現時点では国はそこまではやらないだろうという前提です。
この考え方に基づいて表5前提1を採用し試算したものが表4です。前回のアナリストレポート(7月14日付け)と比べると数字が大きく異なっていますが、これは前回アナリストレポートでは2017年4月の値下げがないとしたためです。
詳細は後日アナリストレポートで示すつもりです。また、2020年3月期以降の試算は、この期の前後から活発になるであろう併用剤、併用療法の寄与を見込んでいません。前提1、前提2ともに、新規投与人数とBMSからのロイヤルティ収入の増加によって、業績は一定の水準まで波を描きながら拡大すると思われます。ただし、2021年3月期以降の業績拡大には、単剤よりも効果の高い併用剤、併用療法の開発が必要になると思われます。
なお、2017年3月期業績については、2017年3月までにオプジーボの薬価引き下げがあれば、会社予想に対して下方修正の可能性がありますが、2017年4月値下げならば下方修正はないと思われます。上市後にオプジーボの副作用が臨床試験で見られたよりも多いことが判明したため(それでも既存の抗がん剤よりは少ないです)、医師、病院側がオプジーボの投与に慎重になっており、会社側も慎重投与を呼び掛けています。そのため、非小細胞肺がんの新規投与人数は会社予想の15,000人を下回る年間10,000~11,000人のペースです。ただし、会社側が見込んでいた投与中の副作用による脱落、死亡例などが想定よりも少ない可能性があり、投与期間も会社想定よりも伸びている可能性があるため、2017年3月期業績は会社予想に対して若干の上乗せが期待できると思われます。
表4 小野薬品工業の業績試算
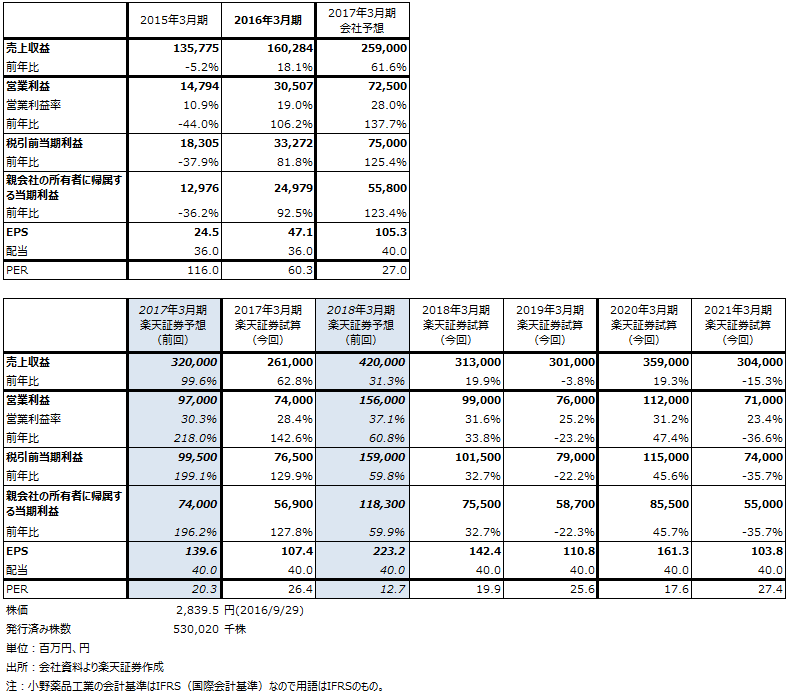
表5 各年度のオプジーボ薬価(月間使用額)の前提

表6 オプジーボの年間新規投与者数の前提
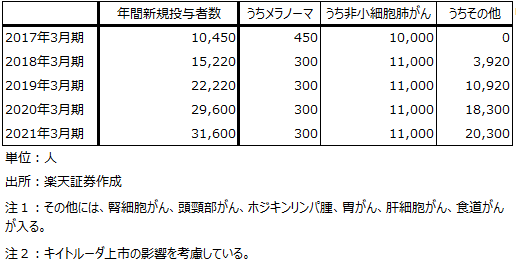
表7 前提1、2に基づく業績試算
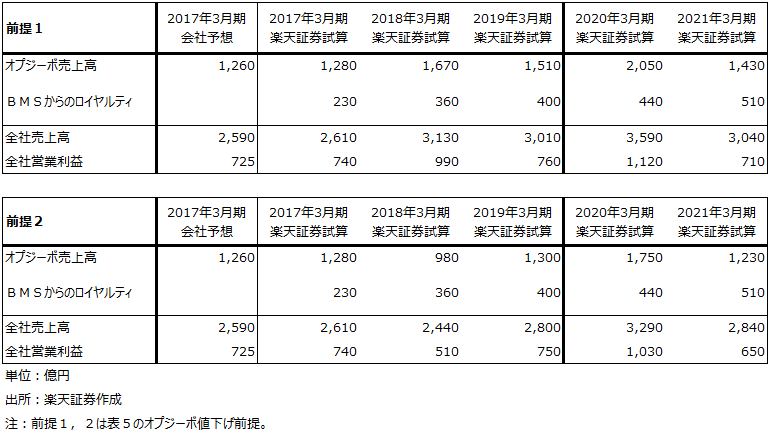
表8 オプジーボ売上高試算(表5前提1の場合)
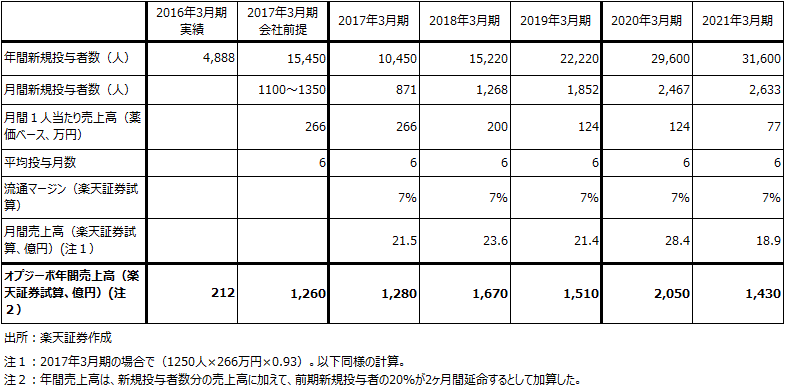
表9 オプジーボ売上高の試算表(表5前提1の場合)
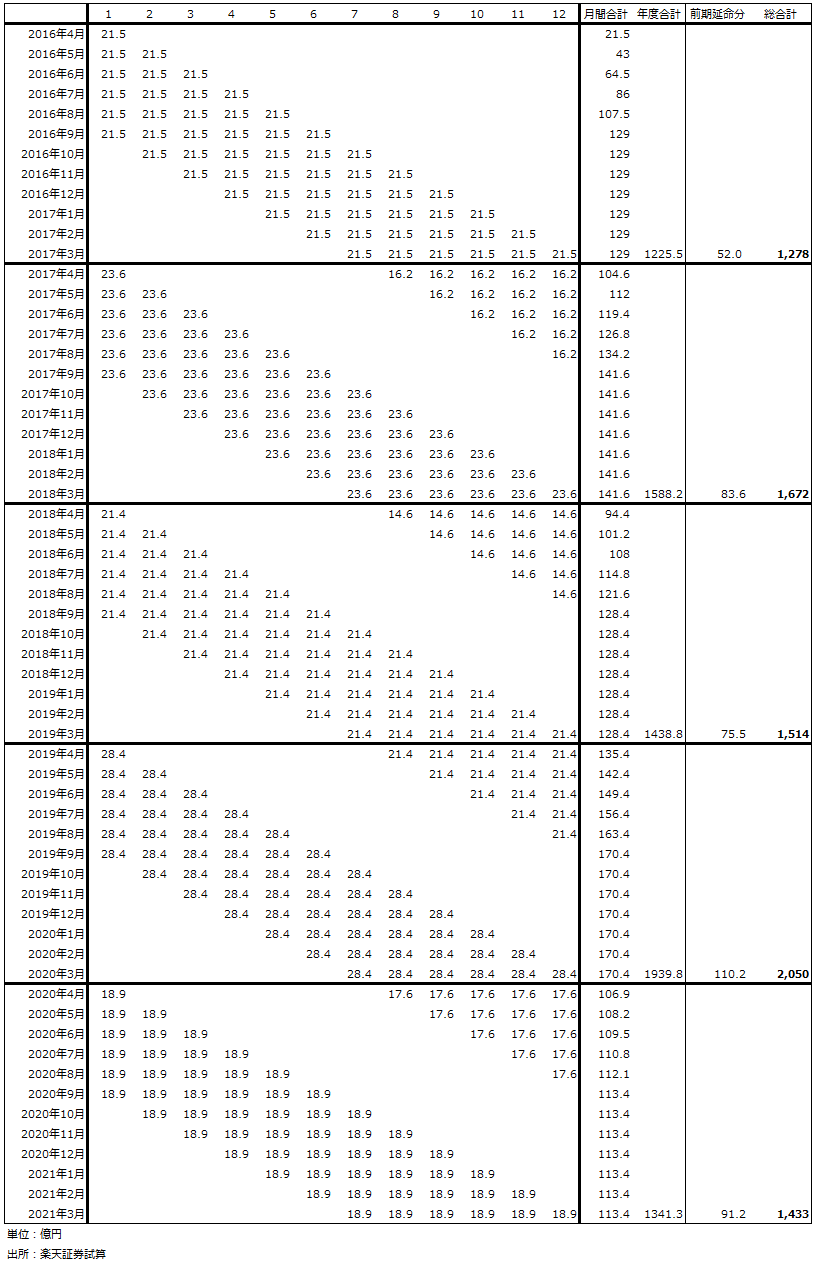
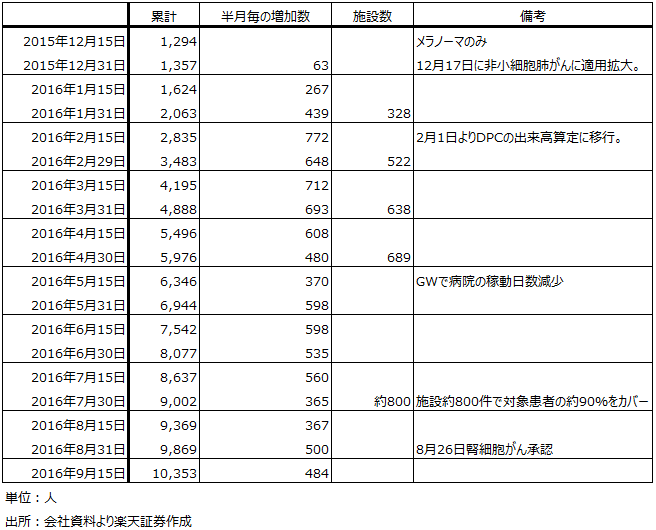
表10 小野薬品工業:オプジーボの累計投与人数
6.株価は一旦戻りの相場か
小野薬品工業の株価は、オプジーボの値下げの議論によって4月から下落が始まり、026試験の失敗という悪材料によって8月以降更に下落しました。これに対して、オプジーボの適応拡大と投与人数の増加は順調に進むと思われることから、業績は波はありながらも一定の利益水準を維持できると思われます。
現在の小野薬品の今期予想PERは26倍ですが、がん領域に熱心な製薬メーカーの今期予想PERを見ると、アステラス製薬が17倍、中外製薬39倍、協和発酵キリン51倍、大塚ホールディングス34倍となっており(数字は9月29日のマーケットスピードによる)、オプジーボのような世界的な超大型新薬を持つ会社としては、小野薬品の26倍は割安と言えます。
株価上の悪材料は、当面は出尽くしたところと思われます。当面は、薬価引き下げ率がどうなるかを見定める必要がありますが、国が小野薬品工業の事業意欲を打ち砕くような大幅値下げをしないならば、株価は一定の戻り(当面は3,500~4,000円のレンジか)が期待できると思われます。
本レポートに掲載した銘柄
小野薬品工業(4528)
本コンテンツは情報の提供を目的としており、投資その他の行動を勧誘する目的で、作成したものではありません。銘柄の選択、売買価格等の投資の最終決定は、お客様ご自身でご判断いただきますようお願いいたします。本コンテンツの情報は、弊社が信頼できると判断した情報源から入手したものですが、その情報源の確実性を保証したものではありません。本コンテンツの記載内容に関するご質問・ご照会等には一切お答え致しかねますので予めご了承お願い致します。また、本コンテンツの記載内容は、予告なしに変更することがあります。
